چرخه اسید سیتریک (چرخه کربس) چیست؟ و چگونه انجام می شود؟ به زبان ساده

چرخه اسید سیتریک (چرخه کربس) چیست؟ و چگونه انجام می شود؟ به زبان ساده
پنهان
چرخه اسید سیتریک که به چرخه کربس یا چرخه تریکربوکسیلیک اسید نیز شناخته میشود، یک مسیر متابولیکی کلیدی در سلولهای هوازی است که نقش اصلی آن تولید انرژی و ترکیبات مورد نیاز برای فرآیندهای زیستی مختلف است. این چرخه در ماتریکس میتوکندری رخ میدهد و با اکسیداسیون استیل – کوآ (حاصل از تجزیه کربوهیدراتها، چربیها و پروتئینها) انرژی شیمیایی را به شکل حاملهای الکترون (NADH و FADH2) ذخیره میکند.
این حاملها سپس در زنجیره انتقال الکترون برای سنتز ATP، که منبع اصلی انرژی سلول است، استفاده میشوند. علاوه بر تولید انرژی، چرخه اسید سیتریک پیشسازهای مهمی برای سنتز اسیدهای آمینه، نوکلئوتیدها و سایر ترکیبات زیستی فراهم میکند و نقش اساسی در تنظیم متابولیسم و رشد سلولی ایفا میکند.
چرخه اسید سیتریک (چرخه کربس) چیست؟
چرخه اسید سیتریک که به عنوان چرخه کربس یا چرخه تریکربوکسیلیک اسید (TCA) نیز شناخته میشود، یکی از مراحل اصلی متابولیسم سلولی در موجودات هوازی است. این چرخه در ماتریکس میتوکندری سلولها رخ میدهد و نقش کلیدی در تولید انرژی به شکل ATP دارد. چرخه اسید سیتریک با ترکیب استیل – کوآ (که از تجزیه کربوهیدراتها، چربیها و پروتئینها حاصل میشود) با اسید اگزالواستیک آغاز میشود و طی چندین واکنش آنزیمی، مولکولهای NADH و FADH2 تولید میشوند.
این مولکولها الکترونها را به زنجیره انتقال الکترون منتقل میکنند و در نهایت موجب تولید ATP میشوند. همچنین، در این چرخه دیاکسید کربن (CO2) به عنوان یک محصول جانبی آزاد میشود. چرخه کربس نه تنها انرژی فراهم میکند بلکه پیشسازهای مهمی برای سنتز اسیدهای آمینه، نوکلئوتیدها و ترکیبات زیستی دیگر نیز تولید مینماید.
کشف و تاریخچه چرخه کربس
چرخه کربس، که بهعنوان چرخه اسید سیتریک یا چرخه تریکربوکسیلیک اسید نیز شناخته میشود، در سال ۱۹۳۷ توسط دانشمند آلمانی، سر هانس آدولف کربس (Hans Adolf Krebs) کشف شد. کربس با مطالعه بر روی متابولیسم سلولهای زنده، بهویژه سلولهای کبدی، به دنبال درک مسیرهای شیمیایی تولید انرژی در موجودات هوازی بود. او از طریق آزمایشهای سیستماتیک با استفاده از بافتهای حیوانی و بررسی تأثیر ترکیبات مختلف بر تنفس سلولی، توانست مسیر حلقهای این چرخه را شناسایی کند.
کربس مشاهده کرد که اسیدهای دیکربوکسیلیک و تریکربوکسیلیک مانند اسید سیتریک، اسید فوماریک و اسید سوکسینیک نقش کلیدی در تولید انرژی دارند و در یک مسیر چرخهای بهطور مداوم تجزیه و بازسازی میشوند. این کشف بهدلیل اهمیت بنیادی آن در درک متابولیسم انرژی، جایزه نوبل فیزیولوژی یا پزشکی را در سال ۱۹۵۳ برای کربس به ارمغان آورد.
پیش از کشف کربس، دانشمندانی مانند آلبرت سنجیورجی نیز به بررسی بخشی از واکنشهای مرتبط با این چرخه پرداخته بودند، اما کربس کسی بود که توانست بهطور جامع مسیر کامل این چرخه را ترسیم و اهمیت آن را در تولید انرژی سلولی اثبات کند. کشف چرخه کربس نقطه عطفی در بیوشیمی و فیزیولوژی سلولی محسوب میشود و بنیانگذار درک مدرن از تنفس سلولی و تولید انرژی در موجودات زنده شد.
مراحل انجام چرخه اسید سیتریک
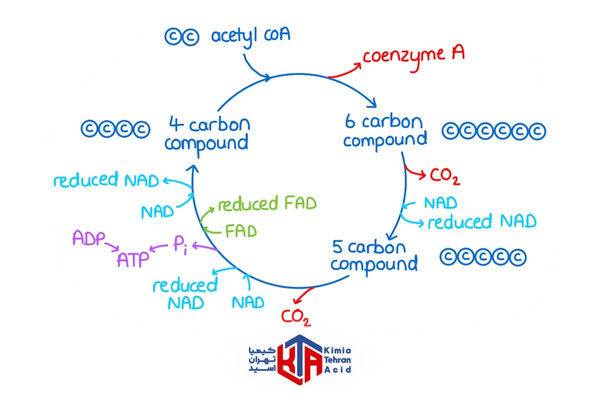
این چرخه از ترکیب استیل-کوآ با اگزالواستات آغاز شده و در طی هشت مرحله پیدرپی، تولید انرژی و ترکیبات میانجی مورد نیاز برای سایر فرآیندهای متابولیکی را فراهم میکند.
در هر دور از این چرخه، دو مولکول دیاکسید کربن، سه مولکول NADH، یک مولکول FADH2 و یک مولکول GTP (یا ATP) تولید میشود که سپس در زنجیره انتقال الکترون برای تولید ATP بیشتر مورد استفاده قرار میگیرند.
۱. تشکیل سیترات (سیترات سنتاز)
چرخه اسید سیتریک با ترکیب استیل – کوآ (یک ترکیب دوکربنه) با اگزالواستات (یک ترکیب چهارکربنه) آغاز میشود. این واکنش توسط آنزیم سیترات سنتاز کاتالیز شده و منجر به تشکیل سیترات، یک ترکیب ششکربنه، میشود. این مرحله یک واکنش بسیار تنظیمشده است و از اهمیت بالایی در کنترل سرعت چرخه برخوردار است. تشکیل سیترات یک واکنش انرژیزا محسوب میشود و موجب حرکت چرخه به سمت جلو میشود.
۲. تبدیل سیترات به ایزوسیترات (آکونیتاز)
سیترات به وسیله آنزیم آکونیتاز به ایزوسیترات تبدیل میشود. این فرآیند در دو مرحله انجام میگیرد: ابتدا سیترات به سیسآکونیتات تبدیل شده و سپس مجدداً تغییر شکل داده و ایزوسیترات را تشکیل میدهد. این تغییر ضروری است، زیرا ایزوسیترات دارای ساختاری مناسب برای اکسیداسیون در مرحله بعدی است.
۳. اکسیداسیون ایزوسیترات و تولید آلفا-کتوگلوتارات (ایزوسیترات دهیدروژناز)
در این مرحله، آنزیم ایزوسیترات دهیدروژناز ایزوسیترات را اکسید میکند و NAD+ را به NADH کاهش میدهد. این واکنش باعث تولید اکسالوسوکسینات میشود که یک ترکیب ناپایدار است و به سرعت به آلفا-کتوگلوتارات (یک ترکیب پنجکربنه) و یک مولکول دیاکسید کربن تجزیه میشود. این اولین مرحلهای در چرخه است که دیاکسید کربن آزاد میشود.
۴. تبدیل آلفا-کتوگلوتارات به سوکسینیل-کوآ (آلفا-کتوگلوتارات دهیدروژناز)
آلفا-کتوگلوتارات در واکنشی که توسط آنزیم آلفا – کتوگلوتارات دهیدروژناز انجام میشود، دچار اکسیداسیون و دکربوکسیلاسیون شده و به سوکسینیل – کوآ تبدیل میشود. این مرحله با تولید یک مولکول دیگر دیاکسید کربن همراه است و همزمان یک مولکول NADH نیز تولید میشود. این واکنش از نظر انرژیزایی قابل مقایسه با واکنش تبدیل پیرووات به استیل-کوآ است و به شدت تنظیم میشود.
۵. تبدیل سوکسینیل-کوآ به سوکسینات (سوکسینیل-کوآ سنتتاز)
سوکسینیل – کوآ توسط آنزیم سوکسینیل – کوآ سنتتاز به سوکسینات تبدیل میشود. این واکنش با آزاد شدن کوآنزیم A (CoA) همراه است و همزمان یک مولکول GTP یا ATP نیز تولید میشود. این مرحله یکی از مراحل کلیدی در چرخه است، زیرا مستقیماً منجر به تولید یک مولکول حامل انرژی میشود که در متابولیسم سلولی نقش دارد.
۶. تبدیل سوکسینات به فومارات (سوکسینات دهیدروژناز)
سوکسینات در واکنش بعدی توسط آنزیم سوکسینات دهیدروژناز اکسید شده و به فومارات تبدیل میشود. این واکنش منجر به کاهش FAD به FADH2 میشود. آنزیم سوکسینات دهیدروژناز در واقع بخشی از زنجیره انتقال الکترون است و در غشای داخلی میتوکندری قرار دارد، جایی که FADH2 مستقیماً الکترونهای خود را به زنجیره انتقال میدهد.
۷. تبدیل فومارات به مالات (فوماراز)
فومارات با افزودن یک مولکول آب، توسط آنزیم فوماراز به مالات تبدیل میشود. این واکنش بدون مصرف ATP انجام میشود و یک مرحله تنظیمی مهم در چرخه محسوب نمیشود، اما برای تکمیل چرخه و ادامه مسیر متابولیکی ضروری است.
۸. تبدیل مالات به اگزالواستات (مالات دهیدروژناز)
در مرحله نهایی چرخه، آنزیم مالات دهیدروژناز مالات را اکسید کرده و به اگزالواستات تبدیل میکند. در این فرآیند، یک مولکول NAD+ دیگر کاهش یافته و به NADH تبدیل میشود. اگزالواستات تولید شده دوباره وارد واکنش با استیل – کوآ شده و چرخه از نو آغاز میشود.
کاربردهای چرخه کربس
چرخه کربس یا چرخه اسید سیتریک یکی از مهمترین مسیرهای متابولیکی در سلولهای هوازی است که نقش حیاتی در تولید انرژی، سنتز ترکیبات زیستی و تنظیم متابولیسم سلولی ایفا میکند. این چرخه علاوه بر تولید ATP از طریق اکسیداسیون استیل – کوآ، پیشسازهای مهمی برای مسیرهای بیوشیمیایی مختلف فراهم میآورد.
تولید حاملهای الکترون (NADH و FADH2) که در زنجیره انتقال الکترون برای سنتز ATP مورد استفاده قرار میگیرند، یکی از کاربردهای کلیدی آن است. همچنین، چرخه کربس در متابولیسم اسیدهای آمینه، گلوکز، اسیدهای چرب و نوکلئوتیدها نقش دارد و ارتباط بین مسیرهای آنابولیک و کاتابولیک را برقرار میکند.
۱. تولید انرژی سلولی (ATP) از طریق زنجیره انتقال الکترون
مهمترین کاربرد چرخه کربس تولید انرژی به شکل ATP است. در طول چرخه، الکترونها بهوسیله مولکولهای حامل NADH و FADH2 جمعآوری میشوند. این حاملها الکترونها را به زنجیره انتقال الکترون در غشای داخلی میتوکندری منتقل میکنند، جایی که الکترونها بهتدریج از طریق مجموعهای از کمپلکسهای پروتئینی عبور داده میشوند. این فرآیند منجر به پمپاژ پروتونها به فضای بینغشایی و ایجاد یک شیب الکتروموتیو میشود.
پروتونها سپس از طریق ATP سنتاز به ماتریکس میتوکندری بازمیگردند و انرژی آزاد شده در این جریان پروتونی برای سنتز ATP از ADP و فسفات معدنی استفاده میشود. هر مولکول NADH حدود ۲.۵ مولکول ATP و هر مولکول FADH2 حدود ۱.۵ مولکول ATP تولید میکند. بهاینترتیب، چرخه کربس بهطور غیرمستقیم سهم عظیمی در تولید انرژی سلولی دارد و بدون آن، سلولهای هوازی قادر به تولید ATP کافی برای حفظ عملکردهای حیاتی خود نخواهند بود.
۲. تأمین پیشسازهای بیوسنتزی برای مسیرهای آنابولیک
چرخه کربس علاوه بر نقش کاتابولیکی در تولید انرژی، یک مسیر آنابولیکی مهم نیز محسوب میشود، زیرا ترکیبات میانی این چرخه بهعنوان پیشسازهای سنتز ترکیبات زیستی مختلف عمل میکنند. برای مثال، آلفا-کتوگلوتارات و اگزالواستات پیشسازهای مهمی برای سنتز اسیدهای آمینه گلوتامات و آسپارتات هستند که خود در سنتز پروتئینها و نوکلئوتیدها نقش دارند.
سوکسینات و فومارات نیز در مسیرهای سنتز پورینها و پیریمیدینها مورد استفاده قرار میگیرند. مالات همچنین میتواند برای سنتز گلوکز از طریق گلوکونئوژنز استفاده شود. این نقشهای بیوسنتزی چرخه کربس را بهعنوان یک پل ارتباطی میان مسیرهای تجزیه و سنتز ترکیبات مختلف معرفی میکند و تضمین میکند که سلولها بتوانند ترکیبات لازم برای رشد و تکثیر را تولید کنند.
۳. متابولیسم و اکسیداسیون اسیدهای چرب و اسیدهای آمینه
چرخه کربس در متابولیسم اسیدهای چرب و اسیدهای آمینه نقش کلیدی دارد. اسیدهای چرب از طریق فرآیند بتا-اکسیداسیون به استیل-کوآ تجزیه میشوند، که مستقیماً وارد چرخه کربس میشود. این فرآیند نقش حیاتی در تولید انرژی از ذخایر چربی بدن ایفا میکند، بهویژه در دورههای روزهداری یا فعالیتهای ورزشی طولانیمدت.
همچنین، بسیاری از اسیدهای آمینه از طریق مسیرهای خاصی به ترکیبات میانی چرخه کربس مانند آلفا-کتوگلوتارات، سوکسینیل-کوآ و فومارات تبدیل میشوند. این فرآیندها به سلول اجازه میدهند تا انرژی موردنیاز خود را از پروتئینها تأمین کند و همچنین پیشسازهای لازم برای بازسازی و سنتز مجدد اسیدهای آمینه را فراهم میآورد. بنابراین، چرخه کربس نقش اساسی در تعادل انرژی و سنتز ترکیبات پروتئینی دارد.
۴. دخالت در گلوکونئوژنز و حفظ سطح گلوکز خون
چرخه کربس بهطور غیرمستقیم در فرآیند گلوکونئوژنز (سنتز گلوکز از ترکیبات غیرکربوهیدراتی) مشارکت دارد. ترکیباتی مانند مالات و اگزالواستات که در این چرخه تولید میشوند، میتوانند از میتوکندری به سیتوپلاسم منتقل شده و در آنجا به فسفوئنول پیرووات تبدیل شوند، که یک ترکیب کلیدی در مسیر گلوکونئوژنز است.
این فرآیند بهویژه در کبد و کلیهها برای حفظ سطح قند خون در دورههای گرسنگی یا بین وعدههای غذایی اهمیت دارد. گلوکونئوژنز تضمین میکند که مغز و گلبولهای قرمز که وابسته به گلوکز بهعنوان منبع انرژی هستند، بهطور مداوم انرژی لازم را دریافت کنند. نقش چرخه کربس در تأمین پیشسازهای این مسیر حیاتی است و نقص در این ارتباط میتواند به اختلالات متابولیکی جدی منجر شود.
۵. تنظیم تعادل انرژی و پاسخ به نیازهای متابولیکی سلول
چرخه کربس نقش اساسی در تنظیم تعادل انرژی سلولی ایفا میکند. سرعت این چرخه بسته به میزان انرژی موردنیاز سلول تنظیم میشود. هنگامیکه سطح ATP بالا باشد، فعالیت آنزیمهای کلیدی چرخه مانند سیترات سنتاز، ایزوسیترات دهیدروژناز و آلفا – کتوگلوتارات دهیدروژناز کاهش مییابد، در نتیجه سرعت چرخه کند میشود.
در مقابل، هنگامیکه سطح ADP و AMP افزایش یابد، این آنزیمها فعال میشوند و سرعت چرخه افزایش مییابد تا تولید ATP بیشتر شود. علاوه بر این، محصولات چرخه مانند سیترات میتوانند بهعنوان سیگنالهای متابولیکی برای تنظیم مسیرهای دیگر عمل کنند؛ بهعنوان مثال، سیترات میتواند مسیر گلیکولیز را مهار و مسیر سنتز اسیدهای چرب را فعال کند. این تنظیمات موجب میشوند که سلول بتواند بهطور مؤثری بین تولید انرژی و سنتز ترکیبات زیستی موردنیاز تعادل برقرار کند.
۶. نقش در تولید ترکیبات ضروری برای استرس اکسیداتیو و دفاع سلولی
چرخه کربس بهطور غیرمستقیم در تولید ترکیبات آنتیاکسیدانی مانند گلوتاتیون نقش دارد. آلفا-کتوگلوتارات و آسپارتات، که از ترکیبات میانی چرخه هستند، در سنتز گلوتامات و سپس گلوتاتیون نقش دارند. گلوتاتیون یکی از مهمترین آنتیاکسیدانهای سلولی است که در محافظت سلولها در برابر استرس اکسیداتیو و آسیبهای ناشی از رادیکالهای آزاد مشارکت دارد.
استرس اکسیداتیو میتواند موجب آسیب به DNA، پروتئینها و لیپیدهای غشایی شود و نقش مهمی در ایجاد بیماریهای مزمن مانند سرطان و بیماریهای قلبی دارد. بنابراین، نقش غیرمستقیم چرخه کربس در حفظ هموستاز اکسیداتیو اهمیت فراوانی دارد و بدون آن، سلولها در برابر آسیبهای اکسیداتیو آسیبپذیر خواهند بود.
۷. مشارکت در سنتز نوکلئوتیدها و متابولیسم DNA و RNA
یکی دیگر از کاربردهای حیاتی چرخه کربس، مشارکت در سنتز نوکلئوتیدها است که برای تولید DNA و RNA ضروری هستند. ترکیبات میانی مانند آسپارتات و فومارات در مسیرهای بیوسنتزی پورینها و پیریمیدینها نقش دارند. بدون این ترکیبات، سلولها قادر به سنتز مواد ژنتیکی لازم برای تقسیم و رشد نخواهند بود.
این کاربرد بهویژه در سلولهایی که دارای نرخ تقسیم بالایی هستند، مانند سلولهای خونی و سلولهای اپیتلیال، اهمیت دارد. همچنین، نقش چرخه کربس در فراهمآوردن پیشسازهای نوکلئوتیدی برای ترمیم DNA به حفظ پایداری ژنومی و جلوگیری از جهشهای ژنتیکی کمک میکند.
مزایا و معایب اجرای چرخه اسید سیتریک
چرخه اسید سیتریک (چرخه کربس) به عنوان یک مسیر متابولیکی مرکزی در سلولهای هوازی، مزایا و معایبی دارد که بر اساس نقش آن در تولید انرژی، تنظیم متابولیسم و تأمین پیشسازهای بیوسنتزی ارزیابی میشوند. این چرخه با فراهم آوردن انرژی و ترکیبات میانجی برای فرآیندهای بیوشیمیایی مختلف، نقش اساسی در بقا و عملکرد سلول دارد، اما در عین حال محدودیتها و نقاط ضعفی نیز دارد که میتوانند بر بهرهوری و پاسخهای متابولیکی سلول تأثیر بگذارند.
مزایا:
- تولید انرژی مؤثر از طریق اکسیداسیون کامل سوختهای زیستی
- تأمین پیشسازهای بیوسنتزی برای اسیدهای آمینه، نوکلئوتیدها و اسیدهای چرب
- مشارکت در گلوکونئوژنز برای حفظ سطح قند خون
- تنظیم تعادل انرژی سلولی از طریق کنترل آنزیمی
- ارتباط مؤثر با زنجیره انتقال الکترون برای سنتز ATP
- پشتیبانی از متابولیسم اسیدهای چرب و اسیدهای آمینه
- فراهمآوری ترکیبات مورد نیاز برای سنتز آنتیاکسیدانها مانند گلوتاتیون
- نقش در تنظیم پاسخهای متابولیکی سلول به استرس اکسیداتیو
معایب:
- وابستگی شدید به اکسیژن برای عملکرد مؤثر
- تولید رادیکالهای آزاد بهعنوان محصولات جانبی و افزایش استرس اکسیداتیو
- کارایی پایین در شرایط بیهوازی
- نیاز به آنزیمهای خاص و شرایط بهینه برای عملکرد صحیح
- مصرف بالای انرژی اولیه برای ورود به چرخه (تبدیل پیرووات به استیل – کوآ)
- احتمال اختلال در عملکرد در صورت کمبود ویتامینها و کوفاکتورهای مورد نیاز
- حساسیت بالا به مهارکنندههای متابولیکی و مواد سمی
- مشارکت در مسیرهای متابولیکی مرتبط با برخی بیماریهای متابولیک و سرطانها
پیشرفتهای پژوهشی اخیر در مطالعه چرخه کربس
در سالهای اخیر، مطالعه چرخه کربس فراتر از نقش سنتی آن در تولید انرژی و متابولیسم پایه سلولی گسترش یافته است. پیشرفتهای علمی و فناوریهای نوین مانند متابولومیکس، ژنومیکس و تصویربرداری پیشرفته سلولی، ابعاد جدیدی از عملکرد و تنظیم این چرخه را آشکار کردهاند. یکی از مهمترین پیشرفتها درک نقش چرخه کربس در تنظیم اپیژنتیک است؛ تحقیقات نشان دادهاند که متابولیتهای میانی این چرخه، مانند آلفا – کتوگلوتارات و سوکسینات، در تنظیم فعالیت آنزیمهای اپیژنتیکی نقش دارند و میتوانند بیان ژنها را از طریق متیلاسیون و دمتیلاسیون DNA و هیستونها تحت تأثیر قرار دهند. این یافتهها نشان میدهد که چرخه کربس نه تنها در تولید انرژی بلکه در تنظیم رشد و تمایز سلولی نیز نقش دارد.
از دیگر پیشرفتهای مهم، بررسی نقش چرخه کربس در سرطان و سایر بیماریهای متابولیکی است. مطالعات اخیر نشان دادهاند که جهش در ژنهای کدکننده آنزیمهای چرخه کربس میتواند به اختلالات متابولیکی منجر شود که در ایجاد و پیشرفت برخی سرطانها نقش دارند. بهعنوان مثال، جهش در ایزوسیترات دهیدروژناز (IDH) باعث تولید متابولیتهای آنومال مانند ۲ – هیدروکسیگلوتارات میشود که میتواند فعالیتهای اپیژنتیکی سلول را مختل کند و موجب سرطانی شدن سلولها شود. این یافتهها منجر به توسعه داروهای هدفمند برای مهار این آنزیمها شده است که در حال حاضر در مراحل آزمایشهای بالینی قرار دارند.
سخن پایانی
چرخه اسید سیتریک، به عنوان هسته مرکزی متابولیسم سلولی در موجودات هوازی، نقش حیاتی در تولید انرژی، تنظیم مسیرهای بیوشیمیایی و تأمین پیشسازهای مولکولی دارد. این چرخه با اکسیداسیون کامل استیل – کوآ، مولکولهای حامل الکترون مانند NADH و FADH2 را تولید میکند که در زنجیره انتقال الکترون برای سنتز ATP، منبع اصلی انرژی سلول، استفاده میشوند. همچنین شما میتوانید برای خرید اسید سیتریک کلیک کنید و با بهترین قیمت آن را تهیه کنید!
علاوه بر تولید انرژی، چرخه اسید سیتریک در تأمین پیشسازهای مورد نیاز برای سنتز اسیدهای آمینه، نوکلئوتیدها و اسیدهای چرب نقش دارد و از طریق تعامل با مسیرهای گلوکونئوژنز و بتا-اکسیداسیون اسیدهای چرب، به حفظ تعادل انرژی و متابولیسم سلولی کمک میکند. همچنین، این چرخه با تنظیم فعالیت آنزیمی بر اساس نیازهای انرژی سلول، در پاسخ به تغییرات محیطی و استرسهای متابولیکی مشارکت دارد.