

اسید کلریدریک جزء مهم ترین مواد شیمیایی صنعتی می باشد.
در بین عموم به جوهر نمک معروف است.
جهت خرید جوهر نمک صنعتی و آزمایشگاهی می توانید با توجه به بسته بندی مورد نظر خرید خود را قطعی کنید
موجود به صورت صنعتی 30 تا 33 درصد و آزمایشگاهی 37 درصد
.
خرید اسید کلریدریک به عنوان محلول آبی یا آبی گازی کلرید هیدروژن HCl که با نام های “جوهر نمک” و “هیدروکلریک اسید ” نیز شناخته میشود، رایج است. در واقع این ماده جز اصلی اسید معده است ، اسیدی که به طور طبیعی در معده انسان تولید می شود و به هضم غذا کمک می کند. همچنین فروش اسید کلریدریک به صورت مصنوعی برای کاربردهای مختلف صنعتی و تجاری صورت می گیرد و می تواند با تعدادی فرآیند تولید از جمله حل گاز کلرید هیدروژن در آب ایجاد شود . قیمت اسید کلریدریک نیز به عنوان یک اسید تحریک کننده خورنده قوی که به صورت گسترده در آزمایشگاه ها نیز استفاده می شود ، متغیر است.
پیشنهاد می شود برای کسب اطلاعات بیشتر درباره این ماده شیمیایی کاربردی و آشنایی با بزرگترین مرجع تخصصی فروش جوهر نمک در ایران با ما همراه باشید.
اسید کلریدریک ،اسیدی بدون رنگ با بویی بسیار تند که در دسته بندی مواد شیمیایی پایه قرار دارد، می باشد. خاصیت خورندگی بالای Hydrochloric acid باعث شده که یک ماده مهم و کاربردی در صنایع به شمار آید. شاید برایتان جالب باشد بدانید که کلریدریک بصورت طبیعی در معده انسان، هنگام صرف غذا ترشح می شود و فرآیند هضم غذا را تسریع می کند.
این ماده به آسانی تبدیل به مایع می شود و در حالت مرطوب یا محلول، ماده آبی رنگ را به قرمز تبدیل می کند. این ماده به علت خواص اسیدی بسیار بالایی که دارد، موارد استفاده عدیده ای را در صنعت به خود اختصاص داده است. موارد مصرف بالای اسید کلریدریک باعث شده تا مراکز فروش مواد شیمیایی نسبت به عرضه آن اقدام کنند. یکی از این مراکز را می توان کیمیا اسید تهران دانست که با سابقه درخشان و طولانی فروش مواد شیمیایی، یکی از برترین مراجع فروش اسید کلریدریک می باشد.

حال که از پرکاربرد بودن این ماده گفتیم، در این مرحله به بررسی مشخصات جزئی تر این محصول می پردازیم و شما را با پاسخ این پرسش که اسید کلریدریک چیست؟ آشنا می کنیم. اسید کلریدریک که آن را با نام های جوهر نمک و اسید معده هم می شناسیم، ماده با فرمول شیمیایی HCL است که دارای بوی تند و زننده و خاصیت اسیدی به شدت قوی است. اسیدیته یا PH این ماده را در حدود 0 تا 2 برآورد می کنند که نشان از قدرتمند بودن این اسید دارد. در پاسخ جزئی تر به این پرسش که اسید کلریدریک چیست؟ باید گفت که این ماده بدون رنگ بوده و به شدت خورنده می باشد. هم چنین به شدت واکنش پذیر است و به ویژه با فلزات واکنش داده و آنها را اکسید می کند. معمولا این ماده را تا غلظت هایی در حدود 30 درصد تولید می کنند. اسید کلردریک با غلظتی در محدوده 30 تا 37 درصد در سامانه فروش کیمیا اسید تولید می شود. البته تولید غلظت های بالاتر امکان پذیر می باشد ولی با توجه به این نکته که به سرعت تبخیر می شود، باید تحت شرایط خاص فشار و دما نگهداری می شود که این امر بسیار هزینه بر و مشکل است. در نتیجه بالاترین درصدی که جوهر نمک تولید می شود به صورت معمول 37 درصد می باشد.

اسید کلریدریک برای اولین بار در حدود 800 سال قبل از میلاد توسط کیمیاگر جابر بن حیان ، با مخلوط کردن نمک معمولی با ویتریول (اسید سولفوریک) کشف شد. جابر بسیاری از مواد شیمیایی مهم را کشف کرد و یافته های خود را در بیش از 20 کتاب ثبت کرد که دانش شیمیایی وی از اسید کلریدریک و سایر مواد شیمیایی اساسی را برای صدها سال را در بر می گرفت. اختراع جابر مورد توجه کیمیاگران بود.
در قرون وسطی ، کیمیاگران اروپایی از اسید کلریدریک به عنوان روح نمک یاد می کردند. HCl گازی را هوای اسید دریایی می نامیدند. نام قدیمی (پیش از سیستماتیک) اسید موریاتیک از همان منشأ است (موریاتیک به معنی “مربوط به آب نمک یا نمک” است) ، و این نام هنوز هم گاهی اوقات استفاده می شود.
کلرید هیدروژن (HCl) یک اسید مونوپروتیک است ، به این معنی که هر مولکول می تواند فقط یک بار جدا شود (یونیزه شود) و یک یون H + (یک پروتون منفرد) آزاد کند.
در اسید کلریدریک آبH + به یک مولکول آب می پیوندد و یک یون هیدرونیوم ، H3O + تشکیل می دهد:
HCl + H2O ⇌ H3O + + Cl−
یون تشکیل شده دیگر Cl− ، یون کلرید است. بنابراین می توان از اسید کلریدریک برای تهیه نمکهایی به نام کلرید مانند کلرید سدیم استفاده کرد. اسید کلریدریک یک اسید قوی است ، زیرا کاملاً در آب جدا می شود.
اسیدهای مونوپروتیک یک ثابت تفکیک اسید دارند ، یعنی Ka ، که نشان دهنده سطح تجزیه در آب است. برای یک اسید قوی مانند HCl ، Ka بزرگ است.
تلاش های نظری برای اختصاص یک Ka به HCl انجام شده است. وقتی نمک های کلرید مانند NaCl به HCl آبی اضافه می شوند ، عملاً هیچ تاثیری بر روی pH ندارند ، این نشان می دهد که Cl− یک پایه مزدوج بسیار ضعیف است و HCl کاملاً در محلول آبی جدا شده است.
شاید دانستن این نکته قبل از خرید جوهرنمک یا اسیدکلریدریک جالب باشد که از بین هفت اسید قوی رایج در شیمی ، که همه آنها غیر آلی هستند، اسید کلریدریک اسید مونوپروتیک است و احتمال دارد تحت واکنش کاهش اکسیداسیون مداخله کننده قرار گیرد،
در واقع اسید کلریدریک یکی از کم خطرترین اسیدهای قوی برای کنترل است.

در این قسمت به آنالیز اسید کلریدریک و بررسی مشخصات ظاهری آن پرداخته ایم. این ماده که در ابتدا در قرن 16 میلادی کشف شد، از حرارت دادن نمک در ظرف های مخصوص ذوب فلزات به دست آمد و به علت خواص عدیده ای که این ماده می توانست در صنعت و به عنوان نوعی واکنش گر داشته باشد، این تولید انقلابی در صنایع شیمیایی نام گرفت. در آنالیز اسید کلریدریک باید گفت که این ماده می تواند در دمای اتاق تولید بخار و گازهای سمی کند که خطرناک بوده و مشکلات تنفسی به همراه خواهد داشت. انواع مختلف صنعتی و آزمایشگاهی از اسید کلریدریک موجود است و موارد استفاده آن از مصارف خانگی تا موارد صنعتی متغیر است.
جدول زیر نشان گر برخی ویژگی های این محصول است که می تواند شما را با این ماده بیشتر آشنا کند.
| نام | اسید کلریدریک، جوهر نمک، اسید معده |
| فرمول شیمیایی | HCL |
| رنگ | بی رنگ |
| بو | بوی تند و زننده |
| PH | 0-2 ، به شدت اسیدی |
| گرید | آزمایشگاهی، صنعتی |
| حالت فیزیکی | مایع شفاف |
هیدروکلریک اسید با حل شدن هیدروژن کلرید در آب تهیه می شود. هیدروژن کلرید را می توان با روش های گوناگونی تولید کرد و این یعنی راه های زیادی برای ساخت اسید کلریدریک موجود است.
در زیر به شرح برخی از آنها می پردازیم تا شما را در تصمیم گیری برای خرید هیدروکلریک اسید مناسب ،راهنمایی کنیم.
شما میتوانید برای اطلاع از روش تولید اسیدکلریدریک مصرفی با کارشناسان مجموعه کیمیا تهران اسید که به عنوان مرجع معتبر خرید و فروش هیدروکلریک اسید شناخته میشوند، در تماس باشید.
اسید کلریدریک اسیدی بدون رنگ با بویی بسیار تند که در دسته بندی مواد شیمیایی پایه قرار دارد. خاصیت خورندگی بالای Hydrochloric acid باعث شده که یک ماده مهم و کاربردی در صنایع بشمار آید. شاید برایتان جالب باشد بدانید که کلریدریک بصورت طبیعی در معده انسان، هنگام صرف غذا ترشح می شود و فرآیند هضم غذا را تسریع می کند. این ماده به آسانی تبدیل به مایع می شود و در حالت مرطوب یا محلول، ماده آبی رنگ را به قرمز تبدیل می کند.

اسید کلردریک 37 درصد با غلظتی در محدوده 30 تا 37 درصد تولید می شود. البته تولید غلظت های بالاتر امکان پذیر می باشد ولی با توجه به این نکته که به سرعت تبخیر می شود، باید تحت شرایط خاص فشار و دما نگهداری می شود که این امر بسیار هزینه بر و مشکل است. در نتیجه بالاترین درصدی که جوهر نمک تولید می شود بصورت معمول 37 درصد می باشد.
شما میتوانید برای استعلام قیمت اسید کلریدریک با کارشناسان فروش ما در ارتباط باشید.
مشتریان میتوانند در هر جای ایران خرید هیدروکلریک اسید را به صورت اینترنتی انجام دهند.
اسید کلریدریک در بدن انسان به عنوان یک جز جدایی ناپذیر در دستگاه گوارش ظاهر می شود.
توسط سلولهای جداری ترشح می شود ، وارد لومن معده می شود و در آنجا به عنوان بخش قابل توجهی از اسید معده عمل می کند.
اسید کلریدریک برای فعال سازی پپسینوژن کار می کند ، در نتیجه آنزیمی به نام پپسین تشکیل می شود. پپسین برای شکستن پیوندهای اسید آمینه در طی فرآیند پروتئولیز کار می کند ، اتفاقی که به طور خلاصه ، به تجزیه پروتئین منجر می شود.
هنگام خرید اسیدکلریدریک تشخیص ظاهر فیزیکی آن به چند طریق ممکن است. این اسید به طور کلی بی رنگ یا کمی زرد است و با بویی مشخص و تحریک کننده ظاهر می شود. در مورد کلرید هیدروژن ، گازی که در اثر برخورد اسید کلریدریک با آب تشکیل می شود ، همین موارد صادق است.
واکنش کاهش اکسیداسیون.
افزودن فلز منیزیم به اسید کلریدریک باعث تولید گاز هیدروژن می شود. منیزیم حل می شود و باعث تشکیل کلرید منیزیم ، MgCl2 می شود.
دانستن این تفاوت برای خرید هیدروکلریک اسید آگاهانه ضروری است.تفاوت اصلی بین اسید کلریدریک و اسید سولفوریک در این است که اسید کلریدریک تک پروتیک است در حالی که اسید سولفوریک دی پروتیک است. اسید کلریدریک و اسید سولفوریک هر دو در کارهای آزمایشگاهی بسیار مهم هستند. از آنجا که آنها اسید هستند ، هنگام دست زدن به این محلول ها باید دقت شود.

HCl اسید قوی تری نسبت به H2SO4 است زیرا یک پروتون به راحتی از یون کلرید جدا می شود تا از یون سولفات هیدروژن و این در ثابت تجزیه آنها منعکس می شود. هرچه مقدار pKa یک اسید کمتر باشد ، قویتر است.
قدرت اسید یکی از عوامل تاثیرگذار در تصمیم گیری درست شما برای خرید هیدروکلریک اسید یا اسید سولفوریک خواهد بود.
اسید سولفوریک تقریباً به طور جهانی برای واکنش های خنثی سازی استفاده می شود. استفاده از HNO3 راحت تر و ایمن تر است و از سایر اسیدها به جز فسفر ، قوی تر است.
شما میتوانید باتوجه به هدف خود از خرید اسید برای راهنمایی بیشتر با مرجع فروش اسید کلریدریک یا اسید سولفوریک تماس حاصل فرمایید.
کلرید هیدروژن یک گاز است و دارای فرمول (HCl (gاست. هنگامی که کلرید هیدروژن در آب حل می شود ، اسید کلریدریک تشکیل می شود. این فرمول یکسانی دارد ، اما شما می توانید تفاوت را به دلیل نماد حالت (aq) ، که مخفف “aqueous” است ، تشخیص دهید. فرمول به صورت( HCl (aq نوشته میشود.
کربنات کلسیم با یک اسید واکنش داده و حبابهایی را روی سطح بلور تولید می کند. برای آزمایش نمونه خود ، اسید کلریدریک رقیق ، آب لیمو یا سرکه را روی نمونه بریزید و مراقب حباب باشید. کوارتز به یک اسید رقیق واکنش نمی دهد.
اگر در هنگام فروش کلریدریک اسید به اطلاعات روی بسته بندی دقت کنید متوجه خواهید شد که کلرید هیدروژن (HCl) ، مخلوطی از عناصر هیدروژن و کلر ، گازی در دمای جو و فشار است. اسید کلریدریک محلول گازی آب در نظر گرفته می شود.
اسید کلریدریک یک ماده فرار است و تقطیر غشایی آن را از محلولهای آن جدا می کند.
اسید کلریدریک ساده ترین سیستم اسیدی حاوی کلر است که حاوی آب است. این یک محلول از کلرید هیدروژن و آب و انواع دیگر گونه های شیمیایی از جمله یون های هیدرونیوم و کلرید است.
محصولات فرعی خطرناکی که در اثر تجزیه اسید کلریدریک ایجاد می شوند عبارتند از: کلرید هیدروژن ، کلر ، مونوکسید کربن ، دی اکسید کربن و گاز هیدروژن.
پس اگر خرید جوهر نمک را به منظور استفاده در آزمایشگاه انجام میدهید،باید حواستان به واکنش های فرعی این ماده شیمیایی باشد.
بخشی از اطلاعات این صفحه از سایت پاب کم برداشت شده است.

کیمیا تهران اسید بزرگ ترین مرجع مواد شیمیایی محصول هیدروکلریک اسید را با بهترین کیفیت در گرید صنعتی و آزمایشگاهی عرضه می کند. جهت ثبت سفارش و اطلاع از قیمت اسید کلریدریک با شماره 02188308030 داخلی بازرگانی تماس حاصل فرمایید.
این ماده به علت خاصیت اسیدی بالایی که دارد و میل به واکنش با ترکیبات دیگر و به ویژه فلزات، کاربردهای عدیده ای در صنعت پیدا کرده است. این کاربردها نه تنها در صنایع شیمیایی است، بلکه در صنایع غذایی هم شاهد استفاده از این ترکیبات هستیم. در ادامه به بررسی کاربرد اسید کلریدریک در بخش های مختلف پرداخته ایم.
تنظیم PH: یکی از موارد مصرف این ماده را می توان جهت تنظیم میزان اسیدی بودن در صنایع غذایی، دارویی و آشامیدنی دانست. برای این منظور مقدار کافی از جوهر نمک را به ترکیبات نام برده برای کاهش اسیدیته استفاده می کنند.

تمیز کاری سرویس بهداشتی: خاصیت خورندگی اسید کلریدریک باعث شده که از آن برای تمیز کردن سطوح حمام و سرویس های بهداشتی و تمامی وسایل چینی استفاده شود. این ماده می تواند جرم ها و مواد آلوده ای که غالبا به سرامیک، چینی و سطوح می چسبد و باعث تغییر رنگ آن می شود را از بین برده و تمیزی و سفیدی را به ارمغان آورد.

شست و شوی استخر: جوهر نمک در غلظت های پایین برای رسوب زدایی و شست و شوی استخرها بسیار مورد استفاده قرار می گیرد. همچنین ماده موثری برای ایجاد سطح بهینه ای از PH می باشد.
تولید کلسیم کلراید: کلریدریک اسید در ترکیب با سنگ آهک واکنشی می دهد که منجر به تولید کلرید کلسیم می شود. این ماده نوعی نمک است که در هنگام بارش برف و یخبندان در سطح جاده به منظور یخ زدایی استفاده می شود.

اسید شویی فلزات: یکی از مهم ترین ویژگی جوهر نمک خاصیت خورندگی بالای این اسید می باشد که می توان از آن برای پاک کردن سطوح فلزی استفاده کرد. در اصطلاح به این فرآیند اسید شویی گفته می شود. در این فرآیند که اصطلاحا اسید شویی نامیده می شود، می توان انواع زنگ زدگی فلزاتی همچون آهن، مس، آلومینیوم و سایر فلزات را پاک کرد و به فلزات تمیز و خالص دست یافت.


جدول زیر نشان گر برخی کاربردهای اصلی کلریدریک اسید در یک نگاه می باشد.
|
کاربردها |
موارد استفاده صنعتی |
گند زدایی از استخرها و تنظیم کننده PH آب |
| استفاده به منظور تولید کلسیم کلراید | ||
| استفاده به منظور اسید شویی فلزات | ||
|
موارد استفاده خانگی
|
تمیز کننده سطوحی نظیر کاشی و سرامیک و چینی | |
| موارد استفاده غذایی | تنظیم کنندگی اسیدیته مواد غذایی و داروها به منظور پیش گیری از فساد |
شما مصرف کنندگان گرامی می توانید برای خرید اسید کلریدریک به سامانه فروش ما مراجعه کرده و نسبت به تهیه این محصول اقدام نمایید. این محصول که در بسته بندی های گالن 5 لیتری صنعتی، گالن 20 لیتری و بشکه 220 لیتری عرضه می شود، دارای کیفیت بسیار بالایی است که می تواند رضایت مصرف کنندگان را به دنبال داشته باشد. خرید اسید کلریدریک با کیفیت بالا در سایت کیمیا تهران اسید امکان پذیر خواهد بود و بهره گیری از کارشناسان همواره پاسخ گو، کار را برای شما مصرف کننده عزیز ساده نموده است. شما می توانید قبل از خرید اسید کلریدریک، نسبت به دریافت مشاوره رایگان اقدام کرده و با آگاهی کامل محصول خود را خریداری نمایید.
یکی از مزیت هایی که سامانه فروش کیمیا اسید به نسبت دیگر مراکز فروش محصولات شیمیایی دارد، قیمت مناسب محصولات است. خرید کلریدریک اسید در این سامانه پایین تر از سایر مراکز می باشد و علت را باید در حذف کردن دست واسطه هایی دانست که باعث افزایش بی دلیل قیمت می شوند. خرید کلریدریک اسید قیمت مناسب در سایت کیمیا تهران اسید، تجربه ای خوشایند است که باعث می شود تهیه کلیه محصولات شیمیایی مورد نیاز خود را به ما بسپارید. شما مصرف کنندگان عزیز می تواند برای اطلاع از قیمت کلریدریک اسید با کارشناسان بخش بازرگانی ما تماس حاصل کنید و ضمن دریافت مشاوره، نسبت به تهیه این محصول در محل خود و در کوتاه ترین زمان ممکن اقدام نمایید.
همان طور که عنوان شد، این ماده دارای خاصیت اسیدی به شدت قوی است و هم چنین واکنش پذیر بودن آن می تواند خطرات جدی را برای سلامتی افرادی که با آن کار می کنند و سلامت محیط کار به همراه داشته باشد. در این قسمت سعی کرده ایم شما را با ایمنی کار با کلریدریک اسید آشنا کرده و خطراتی که حین کار ممکن است بروز کند را عنوان کرده ایم.
استنشاق در محیطی که این ماده در آن وجود داشته باشد، می تواند سبب تحریکات تنفسی شدید شده و زخم گلو، سختی در تنفس و سرفه را به همراه داشته باشد. جوهر نمک در حالت عادی و در دمای محیط می تواند بخارات سمی خود را منتشر کرده و سبب آسیب به مخاط تنفسی گردد.
تماس پوستی با این ماده می تواند سبب خوردگی شدید پوست شود و قرمزی، تاول، درد و سوختگی شدید را به همراه داشته باشد. علت را باید در خاصیت اسیدی شدید این ماده جست و جو کرد. تماس چشمی این ماده هم به شدت خطر آفرین بوده و می تواند سبب سوختگی چشم ها، تحریکات شدید و کوری شود.
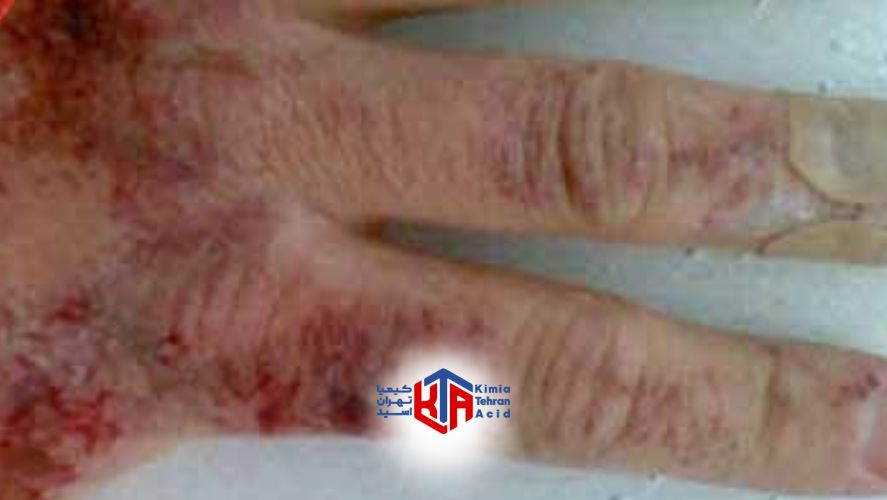
در نهایت بلعیدن این ماده می تواند زخم های شدید و خورنده ای را در مجرای گوارشی از دهان و لب ها تا مری و معده به همراه داشته باشد. ایجاد مشکل به هنگام غذا خوردن و بلع، استفراغ، عطش، حالت تهوع، اسهال، کما و مرگ از عوارضی است که خوردن کلریدریک اسید به همراه خواهد داشت.
جدول زیر نشان گر عوارض مسموم شدن با کلریدریک اسید می باشد.
| مسمومیت با کلریدریک اسید | علائم |
| استنشاق | تنگی نفس، حالت خفگی، تحریکات شدید تنفسی، سرفه و سوختگی گلو |
| تماس پوستی | سوزش و التهاب شدید، قرمزی، سوختگی |
| تماس چشمی | سوختگی شدید، کوری |
| بلعیدن | سوختگی اندام های گوارشی، اسهال، استفراغ، تهوع، کما و مرگ |
برای جلوگیری از بروز صدماتی که عنوان شد، لازم است تا نکات و احتیاط در مصرف به هنگام کار با این ماده اطلاع رسانی شود و از بروز چنین صدماتی پیشگیری به عمل آید. با این حال در ادامه نکاتی مطرح می شود که در صورت وقوع حادثه می تواند به کمکتان آید.
در صورتی که فرد در معرض تنفس این ماده قرار گرفت، فورا وی را به هوای آزاد منتقل کنید و اجازه دهید تا تنفس کند. ممکن است علائم مسمومیت با این ماده خود را پس از 48 ساعت نشان دهد و به همین دلیل مراجعه به پزشک برای پیشگیری و درمان مشکلات تنفسی احتمالی از اهمیت ویژه ای برخوردار است.
در صورتی که فرد در معرض تماس پوستی با جوهر نمک قرار گرفت، موضع را فورا با آب ولرم و تمیز و برای مدت 20 تا 30 دقیقه بشویید و در اولین فرصت نسبت به مراجعه حضوری به پزشک اقدام نمایید. تماس چشمی با این اسید هم نیازمند شست و شوی 20 تا 30 دقیقه ای با آب فراوان است و ضروری است تا پلک ها باز نگاه داشته شوند. بلافاصله باید نسبت به مراجعه به پزشک اقدام نمود.
اگر با فردی مواجه شدید که اسید کلریدریک را بلعیده است، ابتدا دهان وی را بشویید. اگر برای فرد مقدور است، میزان 240 تا 300 میلی لیتر آب به او بدهید و پس از آن به او شیر بخورانید. هرگز چنین فردی را وادار به استفراغ نکنید و اگر خودش استفراغ کرد مجدد به وی آب بدهید. مراجعه فوری به پزشک را در اولویت قرار دهید.
جدول زیر راه کاری هایی موثر در برخورد با فردی که دچار مسمومیت با کلریدریک اسید شده را نشان می دهد.
| مسمومیت با کلریدریک اسید | درمان ها |
| استنشاق | انتقال بیمار به هوای آزاد، انتقال به مراکز درمانی |
| تماس پوستی | شست و شوی موضع با آب فراوان برای مدت 20 تا 30 دقیقه، خارج کردن لباس های آلوده از تن، مراجعه به پزشک |
| تماس چشمی | شست و شوی فوری چشم با آب فراوان برای مدت 20 تا 30 با پلک باز، مراجعه به پزشک |
| بلعیدن | خوراندن آب به بیمار، خوراندن شیر به بیمار، مراجعه فوری به پزشک |
برای پیشگیری از بروز چنین مشکلاتی توصیه می شود به هنگام کار با اسید کلریدریک از پوشش های مناسب کار در محیط های آزمایشگاهی و صنعتی بهره گرفته شود. استفاده از عینک مخصوص، دستکش، لباس مناسب و چکمه می تواند آسیب های پوستی را به حداقل برساند. هم چنین استفاده از ماسک های مخصوص تنفسی برای کاهش صدمات ناشی از بخارات سمی این ماده ضروری است. جوهر نمک خطر آتش سوزی نداشته، اما تماس آن با فلزات می تواند تولید گاز هیدروژن کند که در تماس با هوا می تواند سبب بروز آتش سوزی و انفجار شود. بنابراین در نگه داری آن باید دقت نمود تا از تماس آن با فلزات دوری جسته شود. نگه داری از این مایع در ظروف سر بسته می تواند ضمن جلوگیری از انتشار بخارات سمی، درصد بروز حادثه را به حداقل برساند.
هیدروکلریک اسید در درجه اول در چندین صنعت مانند لاستیک ، منسوجات و حتی در عکاسی یافت می شود. همچنین خرید جوهر نمک برای استفاده خانگی رایج است.
از نظر صنعتی ،افراد برای پردازش فولاد ، تولید باتری ، آتش بازی و موارد دیگر نیز به مراجع فروش اسیدکلریدریک مراجه میکنند.
حال بیایید با جزئیات به برخی از کاربردهای HCL نگاهی بیندازیم تا با توجه به هدف خود به تصمیم قاطعانه تری برای خرید هیدروکلریک اسید برسیم:

اسید کلریدریک / اسید موریاتیک چندین کاربرد صنعتی دارد و یکی از این کاربردها در تولید ترکیبات آلی مانند دی کلرواتان و وینیل کلراید برای PVC است. این ماده همچنین در تولید سایر ترکیبات آلی مانند بیسفنول A ، دی کلرید اتیلن (EDC) که در محصولات مختلف دارویی و صنعت استفاده می شود ، مورد استفاده قرار می گیرد.
بیسفنول A در تولید پلاستیک های پلی کربنات و رزین های اپوکسی مورد استفاده قرار می گیرد اما به دلیل اثرات سرطان زا ، منبع ایجاد ترس در سلامتی بوده است .
به همین دلیل ، توجه به این نکته در هنگام فروش هیدروکلریک اسید ضروری است که بسیاری از پلاستیک ها اکنون به عنوان محصولات فاقد BPA تولید و تبلیغ می شوند. همه این ترکیبات آلی به صنعت پلاستیک و به عنوان حلال آزمایشگاهی کمک می کنند اما می توانند بسیار سرطان زا باشند.
اسید کلریدریک / اسید موریاتیک بسیار مورد استفاده قرار می گیرد ، در واقع خرید اسیدکلریدریک برای استفاده در تولید ترکیبات غیر آلی مواد شیمیایی تصفیه آب، مانند کلرید پلی آلومینیوم (PAC) و کلرید آهن (III) ، اسید فریک که به عنوان عوامل انعقادی و لخته سازی در تولید آب آشامیدنی ، تصفیه فاضلاب و تولید کاغذ استفاده می شوند، رایج است.
این ماده همچنین در بازسازی رزینهای تبادل یونی مورد استفاده قرار می گیرد و به طور خاص برای شستشوی کاتیون ها از رزین ها استفاده می شود.
اگرچه جوهرنمک بسیار خورنده است ، اما برای از بین بردن لکه های فلزات استفاده می شود. این می تواند آهن ، مس ، برنج و سایر فلزات را تمیز کند. اغلب به شکل رقیق شده استفاده می شود. در واقع باید پس از خرید هیدروکلریک اسید آن را با افزودن 9 قسمت آب به 1 قسمت اسید رقیق کرد. نباید از آن به طور مستقیم روی فلزات استفاده کرد زیرا ماده تمیز کنندگی بسیار قدرتمندی است.
اسید کلریدریک معمولاً برای تمیز کردن کاشی در آشپزخانه و حمام استفاده می شود و همچنین فروش اسیدکلریدریک به عنوان ماده ضد عفونی کننده کامل رایج است. همچنین در صنعت نساجی برای سفیدکردن لباس و فرآوری چرم در صنعت برنزه سازی چرم استفاده می شود.

تا اینجا با برخی از کاربردهای محبوب اسید هیدروکلریک آشنا شدیم. برای کسب اطلاعات بیشتر در مورد خواص و ساختار اسیدها و بازها می توانید به صفحه ویکی پدیای این محصول مراجعه کنید یا از طریق شماره های موجود با کارشناسان متخصص کیمیا تهران اسید در تماس باشید.
اگرچه استخرها را می توان با مواد شوینده و اسکراب معمولی تمیز کرد ، اما پاک کردن برخی از لکه ها که بین کاشی ها چسبیده اند کار آسانی نیست. در این صورت ، خرید اسید کلریدریک/ اسید موریاتیک مفید است. همچنین ، باید 10 قسمت آب به 1 قسمت اسید اضافه کنید تا یک محلول رقیق برای تمیز کردن استخر داشته باشید.


یکی از اهداف فروش هیدروکلریک اسید تنظیم اسیدیته (pH) محلول ها است. در واقع برای کنترل PH محصولات دارویی ، غذاها و آب آشامیدنی و همچنین برای خنثی سازی جریان های زائد (حاوی مواد قلیایی) از این ماده شیمیایی استفاده می شود.
این ماده در بازسازی رزینهای تبادل یونی مورد استفاده قرار می گیرد .در واقع این ماده شیمیایی برای شستشوی کاتیون ها از رزین ها استفاده می شود. مبدل های آب و یون معدنی شده در تولید آب آشامیدنی ، کلیه صنایع شیمیایی و بسیاری از صنایع غذایی کاربرد دارند.
تا زمانی که متخصصان با بسیاری از کاربردهای صنعتی جوهرنمک آشنا نبودند، اسید کلریدریک در مایعات حل شده و در دریا ریخته می شد !
از دیگر کاربردهای این ماده شیمیایی میتوان به موارد زیر اشاره کرد:
معده محل مراحل اولیه هضم غذا است.
در بدن انسان ، HCl توسط سلولهای جداری مخاط معده تولید می شود.
سیتوپلاسم سلول جداری با ترکیب آب و دی اکسید کربن باعث تولید اسید کربنیک می شود.
آنزیم کربنیک آنیدراز یک یون اسید کربنیک را به یون هیدروژن منفرد (H +) و یون بی کربنات منفرد (HCO3–) تبدیل می کند.
یون هیدروژن از طریق کانال H + – K + ATPase به معده منتقل می شود و یون های پتاسیم خارج سلولی مثبت را با یون های هیدروژن داخل سلولی مثبت رد و بدل می کنند.
همزمان ، یونهای بی کربنات از طریق مبدل آنیونی که یونهای بی کربنات را با یونهای کلرید منفی مبادله می کند ، از سلول به داخل خون منتقل می شوند.
سلولهای جداری همچنین در غشای خود کانالهای کلرید دارند.
با افزایش غلظت های داخل سلولی ، یون های منفی کلرید به معده منتقل می شوند.
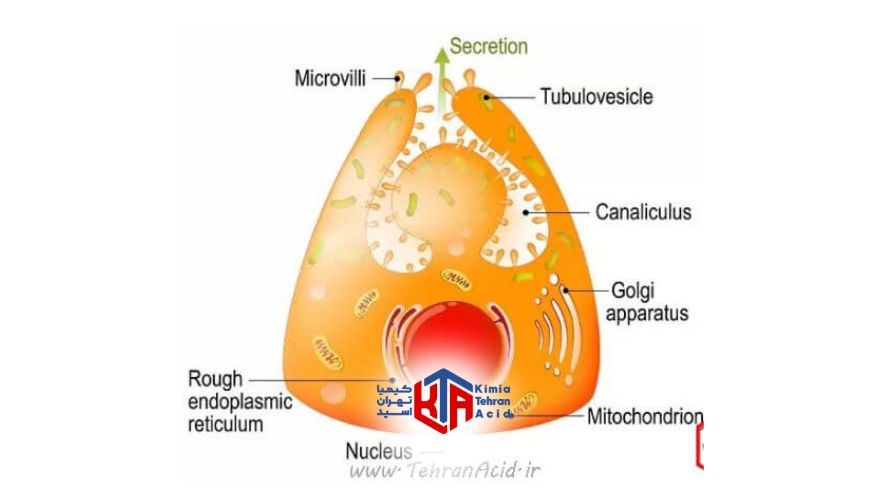
این فرآیند منجر به وجود یون های هیدروژن و کلرید در معده می شود.
آنها به عنوان یونهای منفی و مخالف ، اسید کلریدریک را جذب و تشکیل می دهند. اسید کلریدریک یکی از اجزای مهم آب معده است که برای از بین بردن طیف وسیعی از باکتریهای بیماریزا قبل از فعالیت محتوای معده در محیط جذب بسیار زیاد روده لازم است.
بدن انسان می تواند تولید اسید کلریدریک را به دلیل تحریک عصبی غیر ارادی تنظیم کند.
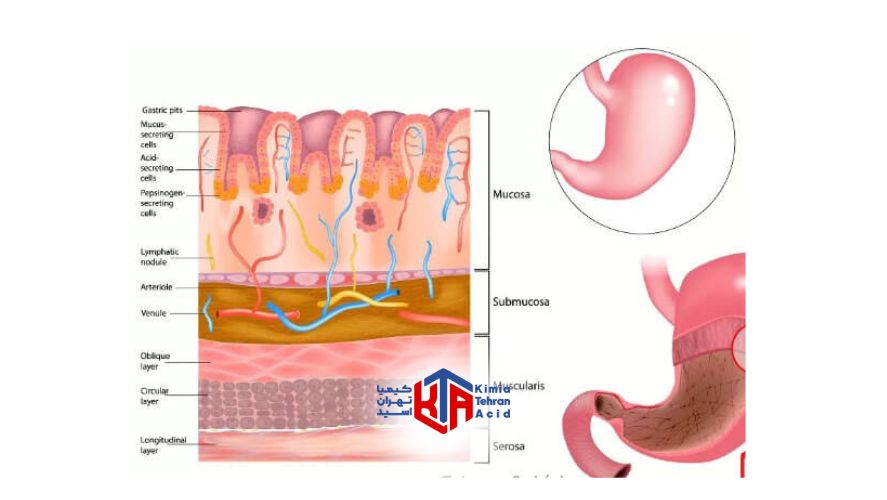
اثر مخالف – کاهش تولید اسید کلریدریک – طی دوره های گرسنگی رخ می دهد که هیچ غذایی در معده وجود ندارد و اسیدیته افزایش می یابد. اسیدیته بالا باعث دفع هیدروژن و یون کلرید در سلول جداری می شود.
همچنین باعث تحریک سلول های D برای تولید سوماتوستاتین می شود که تولید هورمون گاسترین را کاهش می دهد.
عبور مواد غذایی به دوازدهه همچنین باعث ایجاد رفلکسی می شود که به آن رفلکس آنترواگاستریک معروف است ،

استفاده از اسید هیدروکلریک در جنگ معمولاً با تولید و اثرات گاز خردل یا خردل گوگردی که در جنگ خندق در جنگ جهانی اول استفاده می شود ، ارتباط دارد ،
با این وجود اخیراً در جنگ داخلی سوریه مورد استفاده قرار گرفته است ،
حتی اگر استفاده از سلاح های شیمیایی ممنوع باشد با فروش اسیدکلریدریک میتوان باعث ایجاد تاول روی پوست و غشاهای مخاطی دستگاه تنفسی شد .در واقع به دستگاه گوارش حمله کرده و باعث سوختگی ، تورم ، تحریک و تاولهای چرکی می شود. گاز خردل همچنین باعث جهش در DNA می شود و یک ماده سرطان زا شناخته شده است. پادزهر وجود ندارد.
جهت تنظیم میزان اسیدی بودن در صنایع غذایی، دارویی و آشامیدنی استفاده می شود.
خاصیت خورندگی اسید کلریدریک باعث شده که از آن برای تمیز کردن سطوح حمام و سرویس های بهداشتی و تمامی وسایل چینی استفاده شود.
جوهر نمک در غلظت های پایین برای رسوب زدایی و شست و شوی استخر ها بسیار مورد استفاده قرار می گیرد. همچنین ماده موثری برای ایجاد سطح بهینه ای از PH می باشد.
در ترکیب با سنگ آهک واکنشی می دهد که منجر به تولید کلرید کلسیم می شود. این ماده نوعی نمک است که در هنگام بارش برف و یخبندان در سطح جاده به منظور یخ زدایی استفاده می شود.
یکی از مهم ترین ویژگی جوهر نمک خاصیت خورندگی بالای این اسید می باشد که می توان از آن برای پاک کردن سطوح فلزی استفاده کرد. در اصطلاح به این فرآیند اسید شویی گفته می شود. در این فرآیند که اصطلاحا اسید شویی نامیده می شود، می توان انواع زنگ زدگی فلزاتی همچون آهن، مس، آلومینیوم و سایر فلزات را پاک کرد.
و دیگر کاریردها :
باید هنگام خرید اسید کلریدریک دقت کرد تا به همراه آن کاتالوگ طریقه استفاده از آن دریافت و مطالعه شود و در هنگام فروش اسید کلریدریک به مشتری تمام نکات تکمیلی گفته شود.
اسید کلریدریک به عنوان یک ماده سمی شناخته شده و تنظیم می شود. مه اسیدی ممکن است حاوی اسید کلریدریک غلیظ باشد که به عنوان بخار اسید کلریدریک شناخته می شود. این غبار و محلول دارای اثر خورنده ای بر روی بافت انسان است ، با توانایی آسیب رساندن غیرقابل برگشت به اندام های تنفسی ، مو ، پوست و روده ها.
پس حتما در هنگام خرید و فروش اسیدکلریدریک تمام نکات ایمنی رعایت شود.
اسید کلریدریک یک مایع خطرناک است و دارای برگه اطلاعات ایمنی مواد (MSDS) است که باید در هنگام فروش هیدروکلریک اسید در اختیار شما قرار داده شود.
این اطلاعاتی است که فاکتورهای ایمنی و بهداشت شغلی مربوط به استفاده از آن را ذکر می کند، در مکانی که مواد بالقوه خطرناک یافت می شود، باید در دسترس باشد و بتوان آنها را به راحتی پیدا کرد.

هنگام استفاده از HCl برای محافظت از چشم و پوست خود ، همیشه از یک پیش بند مقاوم در برابر مواد شیمیایی ، دستکش های مقاوم در برابر مواد شیمیایی و عینک های محافظ شیمیایی، چکمه های لاستیکی استفاده کنید. اسید کلریدریک غلیظ در صورت استنشاق سمی است ، بنابراین از تنفس آن اجتناب کنید .
علاوه بر این ، هر محوطه ای که از اسید کلریدریک استفاده شود باید به سیستم برافروختگی چشم دسترسی داشته باشد.
حتی هنگام تمیز کردن در خانه با محصولات رقیق شده ، پاشیدن این ماده به چشم یا پوست می تواند باعث سوختگی شود.
توصیه MSDS درمورد تماس اسید کلریدریک با پوست شامل شستشوی محل به مدت حداقل 15 دقیقه و از بین بردن هرگونه لباس که با محلول تماس پیدا کرده باشد.
در مواردی که سوختگی قابل مشاهده است ، شستن با صابون ضد باکتری یا استفاده از کرم ضد باکتری توصیه می شود ،
همچنین مراجعه به یک مرکز پزشکی. تماس با چشم نیاز به یک سیستم گرگرفتگی دارد که حداقل برای 15 دقیقه چشم آسیب دیده را شستشو می دهد و نیاز به مراقبت پزشکی دارد.
مصرف اسید کلریدریک از هر غلظت می تواند باعث سوختگی داخل دهان ، گلو و مری شود. این اتفاق ممکن است زمانی رخ دهد که آب معده بسیار اسیدی باشد و در مخزن معده باقی مانده باشد.
سوهاضمه ناشی از بالا رفتن اسید معده به مری تحتانی می تواند خطر سرطان مری را افزایش دهد. یک اختلال شایع در دستگاه گوارش بیماری رفلاکس معده یا مری یا ریفلاکس است.
تصویر زیر علائم و نشانه های این آسیب شناسی اغلب دردناک را نشان می دهد.
اگر HCl بلعیده شود مهم نیست که استفراغ کنید بلکه در عوض به دنبال مراقبت های پزشکی فوری باشید.
استنشاق غبار HCl نیز نیاز به مراجعه به بخش اورژانس دارد.
قرار گرفتن پوست در معرض غلظت کم گاز هیدروژن کلرید یا اسید کلریدریک باعث التهاب پوست می شود در حالی که غلظت زیاد می تواند باعث سوختگی شدید شیمیایی پوست و غشاهای مخاطی شود.
اسید کلریدریک را با یک قلیایی (باز) ، مانند بی کربنات سدیم (جوش شیرین) خنثی کنید. با پوشیدن لباس های محافظ خود و کار در یک مکان تهویه به دور از کودکان ، حیوانات خانگی ، گرما و فلزات ، یک مخلوط پایه تهیه کنید. 1 پوند جوش شیرین را با آب فراوان مخلوط کنید.
مصرف اسید کلریدریک غلیظ می تواند باعث درد ، مشکل در بلع ، حالت تهوع و استفراغ شود. بلع اسید کلریدریک غلیظ همچنین می تواند باعث آسیب شدید خورنده در دهان ، مری گلو و معده شود ، همراه با خونریزی ، سوراخ شدن ، ایجاد زخم یا تشکیل تنگی به عنوان عوارض احتمالی.
پس از خرید هیدروکلریک اسید، آن را از دسترس کودکان دور نگه دارید.
غیر قابل احتراق است اما کاربید کلسیم با گاز سدیم کلرید هیدروژن واکنش نشان می دهد. فسفید اورانیوم با اسید کلریدریک واکنش داده و فسفین قابل اشتعال خود به خود آزاد می شود.
در هنگام فروش هیدروکلریک اسید ،بسته ها را در جای مطمِئن و به دور از سایر مواد شیمیایی نگهداری کنید.
ساده ترین راه برای آزمایش اسید کلریدریک با محلول نیترات نقره است. محلول نیترات نقره را در لوله آزمایش به محلول آزمایش اضافه کرده و واکنش را مشاهده کنید. اگر رسوب سفید ایجاد شود ، اسید کلریدریک وجود دارد.
اگر ظرف باز باشد ، گاز HCl خارج شده و محلول اسید با گذشت زمان رقیق می شود. برخی از اسیدهای آلی نیز از این طریق تحت تأثیر قرار می گیرند. اما ، اسید سولفوریک غلیظ به سختی جدا می شود – یون های هیدروژن آزاد کمی وجود دارد.
پس در هنگام خرید و فروش هیدروکلریک اسید از بسته بودن درب محصول اطمینان حاصل کنید.
تماس با پوست : می تواند سبب تحریکات شدید پوستی، قرمزی، تاول و درد و سوختگی و صدمات پوستی شود.
تماس با چشم : غلظت بخارات، قطرات این ماده میتواند سبب تحریکات شدید، سوختگی و کوری چشم می شود.
بلعیدن و خوردن : میتواند سبب زخم های خورنده در دهان، گلو، مری و شکم می شود. علایم آن شامل سختی در قورت دادن، عطش، استفراغ و حالت تهوع، اسهال، صدمات شدید، اغما و مرگ است.
تنفس : جوهر نمک بسیار خورنده است و تاثیرات آن بستگی به غلظت و مدت زمان تماس دارد. بخارات و میست این ماده می تواند سبب تحریکات شدید بینی، زخم گلو، انسداد، سرفه و سختی شود. در مدت مواجهه با این ماده زخم در بینی و گلو ایجاد می شود
خطر آتش گیری: این ماده نمیسوزد، تماس با فلزات، تولید گاز هیدروژن کرده که مخلوط این گاز با خطر آتش
تماس با پوست: سریعا موضع آلوده را با آب ولرم به مدت 20 تا 30 دققه شستشو داده و به پزشک مراجعه شود.
تنفس: منبع مولد آلودگى يا فرد را به هواى آزاد برده . علائم مسموميت با اين ماده 48 ساعت پس از مواجه نمايان مى شود.
اطلاعات پزشکی: علائم حياتى فرد ( دما، فشارخون و …) را مرتب چك كرده و به پزشك يا نزديك ترين مركز كنترل سموم مراجعه شود.
تماس با چشم: سریعا چشم های آلوده را به مدت 20 تا 30 دقیقه با آب ولرم شستشو داده، پلک ها باز نگه داشته شوند و به پزشک مراجعه شود.
بلعیدن و خوردن: هرگز به فردى كه بيهوش است چيزى نخورانيد. درصورت هوشيارى فرد دهان وى را با آب تميز شستشو داده و فرد را وادار به استفراغ نكنيد . به فرد هوشيار 240 تا 300 ميلى ليتر آب بخورانيد، درصورت امكان پس ازخوردن آب به فرد شير دهيد. اگر استفراغ به صورت طبيعى اتفاق افتاد دوباره به فرد آب داده به پزشك مراجعه شود.
| percent | Analays |
| 30 – 33 > | Assay |
| 0.05 > | Free Chlorine |
| 0.005 > | Sulfate |
| 0.001 > | Heavy metals |
| 0.001 > | ( +phosphate ( po |
| 0.5 > | Residu igni tion |
| 0.01 > | Sulfit |
آنالیز اسید کلریدریک 37 درصد آزمایشگاهی
| 37-35 | Assay |
| ( g/cmol ( 20 C | Density |
| 000.01 => | Free chlorine |
| 000.05 => | Sulphate |
| 00.001=> | Sulfite |
| 000.01 => | Heavy metals |
| 000.01 => | AS |
| 00.001=> | Ca |
| 00.002=> | Fe |
| 0.000004=> | Hg |
| 0.008=> | Residue on ignition |
| 00.005=> | Non Vlatile matter |
اسید کلریدریک
صنعتی 30 تا 33 درصد-آزمایشگاهی 37 درصد
صنعتی / آزمایشگاهی
HCl
3
36.46
1.18
27.32 درجه سانتیگراد
110 درجه سانتیگراد
✔️بشکه 220 لیتری فلزی, ✔️گالن 20 لیتری, ✔️گالن 5 لیتری, بسته 1 کیلوگرمی/1لیتری
اسید کلریدریک رو عمده میخوام سفارش بدم لطفا راهنمایم کنید چجوری سفارش بدم؟
خوبه